O que é carbonato de zinco?
Carbonato de Zinco é um sólido incolor ou branco que se encontra na natureza formando o mineral Smithsonite, no qual pode estar sozinho ou com outros elementos como o cobalto ou o cobre, que lhe conferem a cor violeta ou verde respectivamente. O ZnCO3 é quase insolúvel em água, mas se dissolve facilmente em ácidos diluídos, uma vez que o íon carbonato em meio ácido forma ácido carbônico (H2CO3), que é então convertido em gás CO2 e água. É usado como anti-séptico em feridas de animais e às vezes é fornecido na dieta para evitar doenças causadas pela deficiência de zinco.

Para que é usado o carbonato de zinco?
O Carbonato de Zinco tem muitas aplicações. Os principais estão listados abaixo:
Em aplicações veterinárias
Serve como adstringente, anti-séptico e protetor tópico de feridas em animais.
Também auxilia na prevenção de doenças causadas pela deficiência de zinco, por isso é utilizado como complemento na dieta de alguns animais, desde que as quantidades administradas estejam dentro dos padrões estabelecidos pelas organizações de saúde.
O carbonato de zinco às vezes é administrado como micronutriente para prevenir doenças em animais.

Em tratamentos médicos
Este composto permite a obtenção de alguns produtos farmacêuticos. É aplicado na pele inflamada na forma de pó ou loção.

Como retardador de chama
É utilizado como enchimento à prova de fogo para borrachas e plásticos expostos a altas temperaturas.
Protege as fibras têxteis do fogo. No caso dos têxteis de algodão, é aplicado no tecido junto com um pouco de álcali. Isso ataca diretamente os grupos hidroxila primários (–CH2OH) da celulose e os converte em celulose sódica (–CH2ONa).
A quebra das ligações da celulose pelo álcali favorece uma maior penetrabilidade das cadeias da estrutura celulósica compacta, razão pela qual mais ZnCO3 consegue entrar na zona amorfa desta, e sua dispersão é facilitada.
Alguns tecidos de algodão podem conter ZnCO3 nas suas fibras para torná-los resistentes ao fogo. Como resultado, a quantidade de gás inflamável que poderia ser produzida pelo fogo é reduzida.

Para separar minerais perigosos do arsênico
Métodos de separação de minerais de arsênico de rochas sulfetadas (como galena, calcopirita e pirita) foram testados usando ZnCO3. O mineral rico em arsênico deve ser separado dos demais porque este elemento é um poluente muito tóxico e venenoso para os seres vivos.
Para conseguir isso, a mistura das rochas moídas é tratada com uma solução de sulfato de zinco e carbonato de sódio a um pH de 7,5-9,0 e um composto de xantato.
A eficácia da fórmula é atribuída à formação de pequenas partículas de ZnCO3 na superfície da arsenopirita, tornando-a hidrofílica (relacionada à água), portanto não consegue aderir às bolhas de ar e não pode flutuar, precipitando e separando os demais minerais.
Em tratamentos odontológicos
Certos cremes dentais à base de carbonato de zinco e nanocristais de hidroxiapatita são aplicados regularmente na prótese. Reduz a hipersensibilidade de forma mais eficaz do que aqueles à base de flúor.
Os nanocristais de ZnCO3 e hidroxiapatita possuem tamanho, formato, composição química e cristalinidade semelhantes aos da dentina para que os túbulos dentinários possam ser fechados com a aplicação desses materiais.
Nanopartículas de ZnCO3-hidroxiapatita foram testadas com sucesso para diminuir a sensibilidade em dentes clareados. Este tipo de creme dental é útil após processos de clareamento dental.
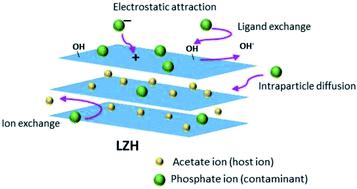
Na Recuperação de Zinco de Efluentes Residuais
Águas sintéticas ricas em íons de zinco descartadas por processos de galvanoplastia podem ser tratadas por tecnologia de leito fluidizado utilizando carbonato de sódio para precipitar ZnCO3.
Ao precipitar o Zn2+ na forma de carbonato, sua concentração diminui, o sólido obtido é filtrado e as águas podem ser descartadas com segurança. O ZnCO3 precipitado é de alta pureza.
O carbonato de zinco é bom para a pele?
O óxido de zinco e o carbonato de zinco, que são altamente insolúveis, são aplicados generosamente na pele inflamada na forma de pó, loção de calamina e semelhantes. Cloreto de zinco, sulfato e acetato têm sido usados por suas propriedades anti-sépticas, adstringentes ou cáusticas. Seu uso é limitado pela dificuldade de controle local e não pelos efeitos sistêmicos. O sulfato de zinco tem sido usado como emético na dose oral de 1.000 ou 2.000 mg em um copo
de água. Esta dose produz intencionalmente uma concentração na água bem acima do limite que pode causar vómitos se tomada com o estômago vazio, como por vezes acontece acidentalmente quando sumo de fruta ou outras bebidas ácidas são armazenados em recipientes galvanizados.
Qual é o método de produção de carbonato de zinco?
O método de produção de carbonato de zinco é principalmente o método de decomposição de compostos, que logo contém matérias-primas de zinco ou óxido de zinco e ação de ácido sulfúrico, a solução bruta de sulfato de zinco, por oxidação de permanganato de potássio, remove ferro, manganês e outras impurezas e, em seguida, adiciona pó de zinco, após agitação pode remover níquel, cobre, cádmio e outras impurezas. Foi então reoxidado com permanganato de potássio para remover pequenas quantidades de manganês e ferro. A solução refinada de sulfato de zinco foi combinada com soda alcalina para formar carbonato de zinco alcalino, e a temperatura de reação foi controlada em 46 ℃, pH 6,8 e álcali livre em 0,4% a 0,5%. O material de pasta obtido por redecomposição, a torta de filtro é seca a 100 ℃, com teor de umidade abaixo de 2,5% e, após moagem fina e peneiramento, produz produtos acabados de carbonato de zinco alcalino.
O carbonato de zinco A é ácido ou base?
O carbonato de zinco é um sal, não um ácido ou um álcali.
Como comprar carbonato de zinco?
Na Qi Di Chem, vendemos carbonato de zinco. O preço do Carbonato de Zinco costuma variar de acordo com o preço da matéria-prima. Para obter o preço mais recente, entre em contato conosco e forneceremos uma cotação adequada para seu país/região. Exportamos para todo o mundo, então você pode entrar em contato pelo e-mail mandy@czqidi.com para um orçamento gratuito ou enviar uma mensagem no WhatsApp para uma resposta rápida +86-186-5121-5887.
Se quiser saber mais informações, clique QiDi Chem para encontrar mais detalhes.
English
العربية
Français
Русский
Español
Português
Deutsch
italiano
日本語
한국어
Nederlands
Tiếng Việt
ไทย
Polski
Türkçe
አማርኛ
ភាសាខ្មែរ
Bahasa Melayu
ဗမာစာ
Filipino
Bahasa Indonesia
magyar
Română
Čeština
қазақ
हिन्दी
فارسی
Kiswahili
Slovenčina
Slovenščina
Norsk
Svenska
українська
Ελληνικά
Suomi
עברית
Latine
Dansk
اردو
বাংলা
Hrvatski
Afrikaans
Eesti keel
සිංහල
latviešu
Български
Hausa
íslenska
Kurdî
Lietuvių
isiZulu














